三陰性乳腺癌化療和PD-L1阻斷劑聯合療法的細胞機制各不相同
三陰性乳腺癌(TNBC)是一種侵襲性強、預后差的乳腺癌亞型,傳統治療對其作用有限。近年來,化療藥物(如紫杉醇和白蛋白結合型紫杉醇)與PD-L1阻斷劑(如正反應)的聯合療法顯示出治療潛力,但其具體機制尚不完全清楚。為了深入理解不同化療藥物與免疫療法聯合時的細胞機制差異,作者通過單細胞RNA測序(scRNA-seq)和T細胞受體測序(TCR-seq),分析了TNBC患者在接受不同聯合治療方案后的免疫細胞動態變化。作者發現,白蛋白結合型紫杉醇(Nab-PTX)與阿特珠單抗(ATZ)聯合治療能夠顯著重塑腫瘤免疫微環境,特別是通過增加肥大細胞和促炎性巨噬細胞的比例,促進T細胞和B細胞的招募和激活。與PTX聯合ATZ相比,Nab-PTX聯合ATZ能夠將CD8+ T細胞從耗竭狀態轉變為具有干細胞特征的記憶效應T細胞(Tsem),同時減少調節性T細胞(Treg)的比例,從而增強抗腫瘤免疫反應。此外,肥大細胞的激活在Nab-PTX聯合治療中發揮了關鍵作用,可能通過促進T細胞和B細胞的招募來增強PD-L1阻斷劑的療效。小鼠模型實驗進一步證實了肥大細胞激活對腫瘤生長的抑制作用。總之,作者的研究揭示了不同化療藥物與PD-L1阻斷劑聯合時多種免疫細胞的動態和肥大細胞在聯合治療中的關鍵作用與具體機制,并為開發新的聯合治療策略提供了理論依據。該研究于2025年1月發表在《Cancer cell》,IF 48.8分。
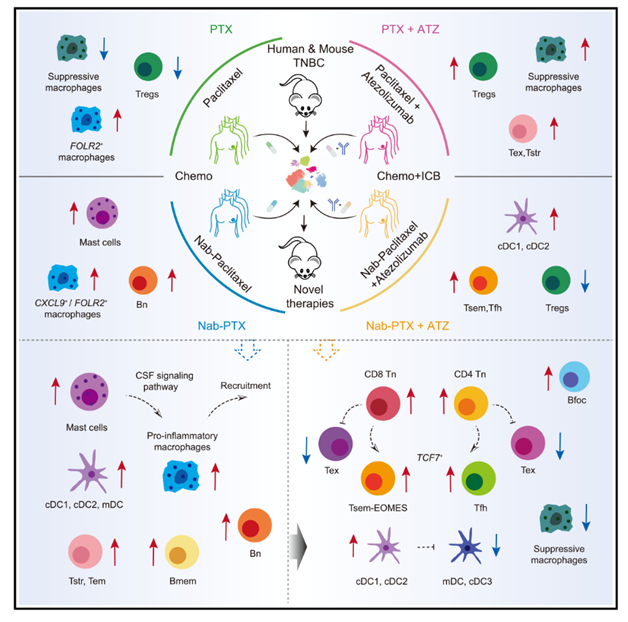
技術路線:
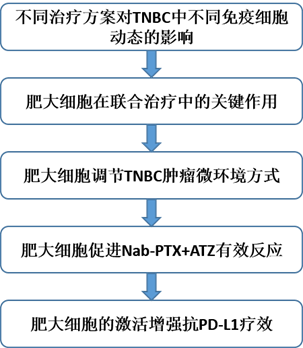
主要研究結果:
1 三陰性乳腺癌(TNBC)中的免疫細胞圖譜及動態變化
作者從44例TNBC患者中獲得了78份腫瘤活檢樣本。其中,16例接受了Nab-PTX聯合ATZ治療,12例接受了Nab-PTX治療,9例接受了PTX聯合ATZ治療,7例接受了紫杉醇治療。根據可獲得性,收集了包括原發性乳腺腫瘤和轉移性病灶在內的腫瘤樣本,并將其分為應答者(R)和非應答者(NR)(圖1A)。
利用scRNA-seq對TNBC中的免疫浸潤進行分析,經過嚴格的質量篩選后,作者共鑒定出285,001個T細胞、87,595個B細胞、18,718個自然殺傷(NK)細胞和56,180個髓系細胞(圖1B)。作者進一步比較了匹配部位的治療前后樣本,分析免疫細胞的動態變化,幫助減少基線差異的影響。盡管樣本量限制了統計學意義,但作者仍觀察到不同治療方案之間存在不同的動態模式(圖1C)。具體而言,PTX治療后T細胞和NK細胞增加,而Nab-PTX+ATZ治療后髓系細胞減少。此外,化療后應答者的T細胞增加(圖1D),而接受Nab-PTX+ATZ治療的應答者中B細胞呈上升趨勢,而在PTX治療后則下降。相比之下,接受Nab-PTX+ATZ治療的應答者中髓系細胞減少,而PTX治療后NK細胞增加。值得注意的是,B細胞在聯合治療的應答者中占主導地位(圖1E)。預測指數(Pi)和治療指數(Ti)分析一致顯示,基線B細胞水平較高與對聯合治療和PTX的正反應相關,而T細胞則是Nab-PTX的有利預測因子(圖1E)。
通過提高聚類分辨率,作者鑒定出CD4+ T細胞、CD8+ T細胞、CD20+ B細胞、濾泡B(Bfoc)細胞、漿細胞(Pc)、CD56+ NK細胞、CD16+ NK細胞、漿細胞樣樹突狀細胞(pDC)、肥大細胞(Mc)以及其他髓系細胞(圖1F)。B細胞亞群表現出較高的Pi,并與對Nab-PTX+ATZ的正反應相關(圖1G和圖1H),而Bfoc和CD4+ T細胞表現出較高的治療指數,表明它們在應答者中增加。根據預測能力和在應答者中的增加趨勢,作者發現CD8+ T細胞和CD16+ NK細胞傾向于在PTX治療后的應答者中增加,而CD4+ T細胞和CD56+ NK細胞與對Nab-PTX的正反應相關。
鑒于樣本量有限,作者采用多色免疫組化(IHC)染色法對16份腫瘤樣本中的CD8+ T細胞、CD4+ T細胞和CD20+ B細胞進行評估,結果與作者的scRNA-seq數據一致(圖1I)。作者還注意到,在Nab-PTX+ATZ治療后,這些細胞在應答性腫瘤中的水平增加,與scRNA-seq觀察到的趨勢一致(圖1J和圖1K)。
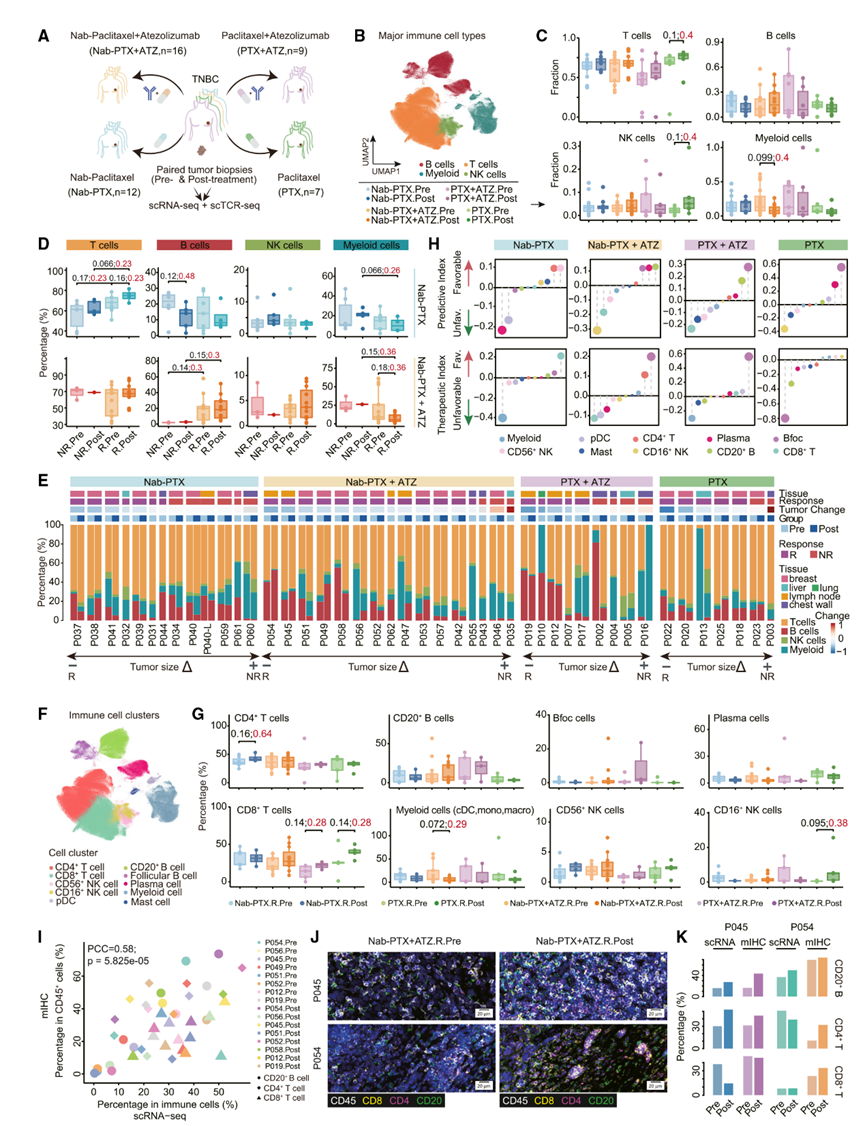
圖1:TNBC中的免疫細胞圖譜及動態變化
2 CD8+ T細胞在不同治療后的差異動態變化
作者在每個主要免疫細胞群內構建了高分辨率圖譜,鑒定出4個以CXCL13和LAG3表達為標志的Tex亞群(圖2A),每個亞群的耗竭標志物、效應標志物和記憶標志物表達水平各有不同。具體而言,Tex-PDCD1和Tex-GZMB表現出較高的HAVCR2和TIGIT水平,以及更高的耗竭評分(圖2A和圖2B)。Tex-GZMB主要富集于與Nab-PTX相關的治療組。對Nab-PTX+ATZ治療有應答的患者Tex-GZMB水平降低,而NR在接受治療后Tex-GZMB水平增加(圖2C、2D)。相比之下,Tex-PDCD1主要富集于與PTX相關的治療組,對PTX+ATZ治療有應答的患者表現出Tex-PDCD1水平上升的趨勢,而對PTX治療有應答的患者在接受治療后Tex-PDCD1水平則呈下降趨勢(圖2C和2D)。對于Tex-ISG15和Tex-MKI67,這兩個亞群均富集于與Nab-PTX相關的治療組,且在接受治療后,應答者的這兩個亞群水平均呈下降趨勢。這些發現表明,Nab-PTX+ATZ治療能夠降低Tex水平,而PTX+ATZ治療與其他治療方案相比,似乎會增加Tex水平。
Tsem在接受聯合治療(尤其是Nab-PTX+ATZ治療)后應答者的水平增加(圖2C、2D)。相比之下,Tisg和Tstr在接受Nab-PTX+ATZ治療后應答者的水平降低,而Tstr在接受PTX或其與ATZ聯合治療后應答者的水平則呈上升趨勢。Tstr以熱休克基因的表達為標志,與對免疫檢查點阻斷(ICB)治療的耐藥性相關。這說明,Nab-PTX+ATZ治療能夠促進一種有益的T細胞狀態,這可能有助于其與其他治療方案相比在臨床中有更好的療效。
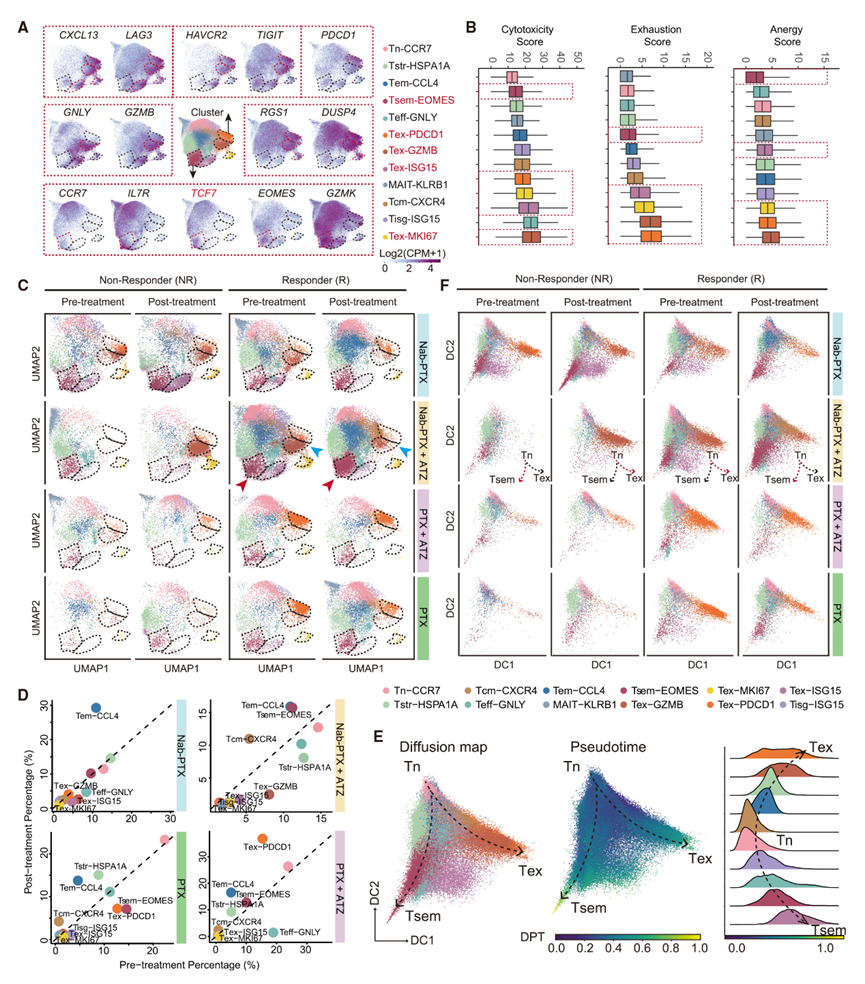
圖2:CD8+ T細胞的組成及動態變化
3 解碼CD8+ T細胞的過渡動態
作者接下來研究了CD8+ T細胞之間的譜系聯系,揭示了兩個分支均源自幼稚T細胞(Tn),分別以耗竭T細胞(Tex)或效應記憶T細胞(Tem)為終端狀態,基于擴散圖分析(圖2E)。在Tex譜系中,Tex-PDCD1和Tex-GZMB位于終端且相互重合,而在Tem譜系中,Tsem伴隨Teff和Tex-ISG15作為終端狀態。譜系的分化可能受到不同治療方案和臨床結果的影響。具體而言,在對Nab-PTX聯合ATZ治療有應答的患者中,治療前腫瘤中Tex譜系占主導地位,而治療后腫瘤則向Tem譜系顯著轉變(圖2F)。而NR在接受治療后則表現出向Tex譜系的富集。這些結果表明,Nab-PTX+ATZ在應答者中有效地阻止了T細胞的耗竭,而在非應答者中,治療對TIME的影響有限,反映了T細胞耗竭的自然進展。
TCR對T細胞的功能至關重要,克隆擴增可以暗示腫瘤抗原的反應性。與先前的研究一致,Tn包含大量的獨特克隆,而Tex和效應T細胞(Teff)表現出高度的克隆擴增(圖3A)。作者還觀察到,有效的Nab-PTX+ATZ治療減少了Tex亞群之間的轉換,同時增強了Tsem的轉換。具體而言,在對Nab-PTX+ATZ治療有應答的治療前腫瘤中,觀察到Tex細胞之間以及Tem與Tn、Tcm和Tstr之間的顯著轉換,而在治療后,觀察到Tsem、Tcm和Tem之間的大量轉換(圖3B和圖3C)。通過定義轉換樞紐性(STAR方法),作者發現這種聯合治療將轉換樞紐從Tn和Tex-GZMB轉移到Tsem和Tem(圖3D)。相比之下,在有效的PTX+ATZ治療后,CD8+ T細胞的轉換動態變化較小。對于化療而言,Tn、Tem和Tsem的轉換樞紐性在有效治療后持續增加(圖3D)。值得注意的是,PTX治療后Tex-PDCD1的樞紐性顯著降低。
綜上所述,作者的研究結果表明,Nab-PTX+ATZ不僅能抑制Tex群體的轉換,而且通過重新配置干細胞樣Tem細胞來實現增強的療效。相比之下,PTX+ATZ似乎只能實現部分效果,導致Tex轉換適度減少,但未能重新配置Tem群體。兩種化療方案對Tem和Tex細胞的影響有限,但傾向于促進Tn細胞的擴增。
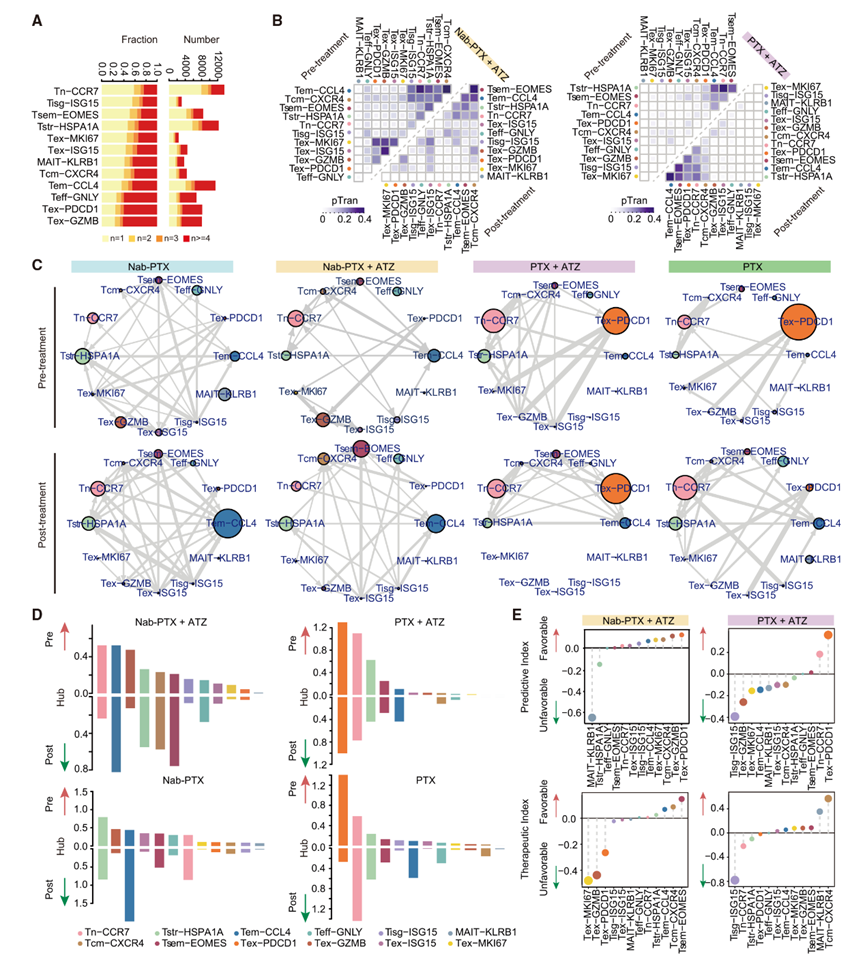
圖3:CD8+ T細胞的過渡動態
4 CD8+ T細胞與臨床反應的關聯
與Pi分析顯示一致,Nab-PTX聯合ATZ治療后,耗竭型CD8+ T細胞(Tex)與臨床正向反應相關,而Tstr與不利的臨床反應相關(圖3E)。與Ti分析結果一致,干細胞樣效應記憶型CD8+ T細胞(Tsem)在應答者中的比例增加,而Tex-GZMB在非應答者中更為常見(圖3E)。這些觀察結果進一步強調了在有效的Nab-PTX+ATZ治療后,效應記憶型CD8+ T細胞(Tem)的擴增以及耗竭型CD8+ T細胞(Tex)的收縮。對于其他治療方案,作者注意到對PTX聯合ATZ治療有應答的患者表現出較高的耗竭型PDCD1+ CD8+ T細胞(Tex-PDCD1)比例,而非應答者在治療前和治療后的樣本中均顯示出較高的干擾素應答型CD8+ T細胞(Tisg)和Tstr比例(圖3E)。
5 鑒定響應性腫瘤浸潤性CD4+ T細胞
隨后,作者將研究重點轉向CD4+ T細胞,發現它們在協調CD8+ T細胞反應中發揮的關鍵作用。作者鑒定出三個Tfh亞群,每個亞群均表達經典的Tfh標記物,如IL6ST、CXCR5和BCL6,但表達水平存在差異(圖4A)。其中Tfh-CXCR5亞群的高表達TCF7與CD4+ T細胞的自我更新相關。CD4+ T細胞的耗竭亞群(Tex)以LAG3、HAVCR2和CTLA4等耗竭標記物為特征,同時表達效應分子,類似于Th1樣細胞。Tex和Tfh亞群均高表達CXCL13和PDCD1(圖4A),表明它們是作者在先前研究中鑒定的CXCL13+ T細胞的組成部分。在Tex、Treg和Tfh亞群中觀察到顯著的克隆擴增(圖4B),這表明它們對腫瘤抗原有反應性。根據STARTRAC分析,這些亞群還表現出較高的轉換指數,并且在Tex-LAG3與Tex-MKI67、Treg-FOXP3與Treg-MKI67之間以及Tex與Tfh之間觀察到活躍的轉換(圖4B)。
Tfh和Tex亞群在應答者中富集,并與聯合治療的正反應相關,而Tstr和Teff在NR中富集,并指示不利結果(圖4C)。Treg在非應答者中富集,與對PTX+ATZ的負反應相關。對Nab-PTX+ATZ有應答的患者表現出Treg、Tex和Tisg水平的降低,以及Tn-IL7R和Tfh水平的增加(圖4D–4F)。相比之下,非應答者表現出Tex水平的增加,以及Tn-IL7R的降低(圖4F)。這些發現表明,Nab-PTX+ATZ降低了Treg和Tex,同時促進了Tfh的擴增。PTX+ATZ增加了Treg和Tstr,另外,Tfh也表現出上升趨勢(圖4D、4E)。兩種化療藥物均與Tfh-DUSP4的增加趨勢和Tex的減少趨勢相關。此外,PTX降低了Treg,而Nab-PTX增加了Tstr水平。
綜上所述,這些發現表明,Tfh的增加以及Treg和Tstr的同步減少對于有效的TNBC治療至關重要。Treg和Tstr可能是影響PTX+ATZ療效的原因。
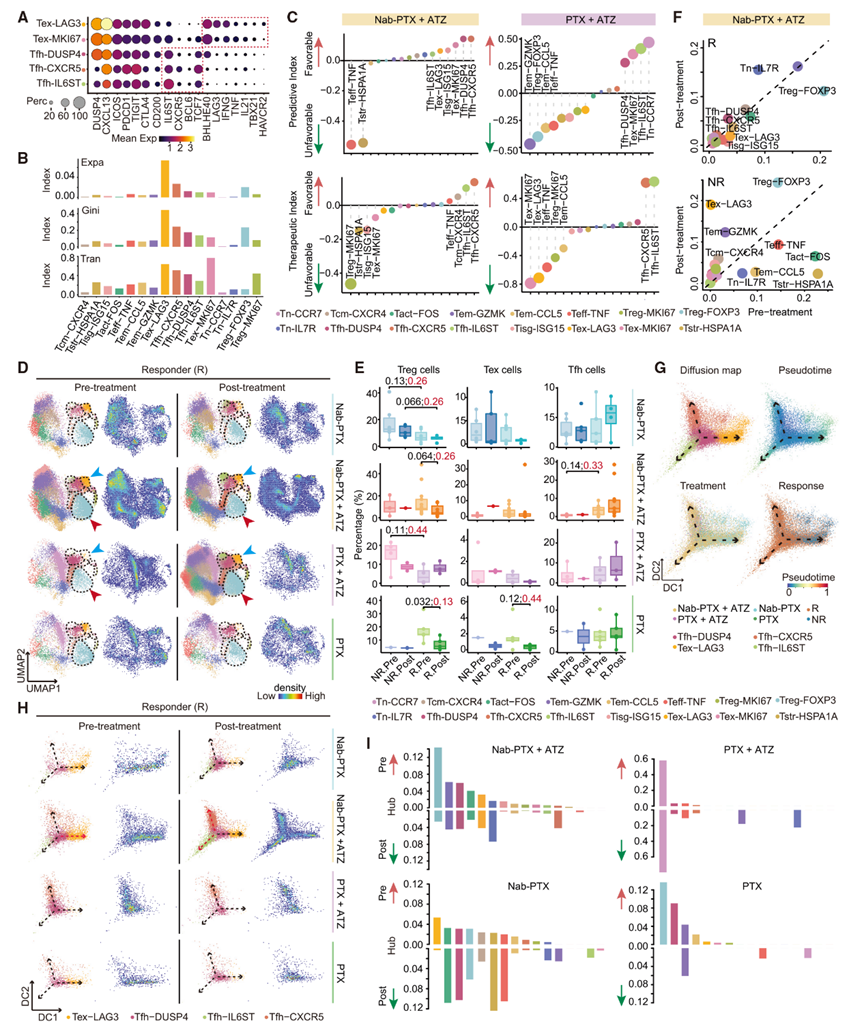
圖4:CD4+ T細胞的組成及動態變化
6 Tfh/Tex的譜系動態及其與臨床反應的關聯
鑒于Tfh/Tex在有效治療中的重要性,作者重建了它們的譜系層次,以闡明潛在的細胞命運可塑性。Tfh-DUSP4被鑒定為過渡態,分化出三個分支,分別以Tex-LAG3、Tfh-CXCR5和Tfh-IL6ST為終端狀態(圖4G)。值得注意的是,對Nab-PTX+ATZ有應答的患者在治療前表現出Tfh-DUSP4和Tex-LAG3的富集,而在治療后則轉變為Tfh-CXCR5和Tfh-IL6ST的富集,而NR在治療后表現出Tex-LAG3的增加(圖4H)。這些觀察結果表明,Nab-PTX+ATZ阻礙了Tfh-DUSP4向Tex的分化,而是將其偏向Tfh方向。相比之下,有效的PTX+ATZ治療僅顯示出從Tfh-DUSP4到Tfh-CXCR5的輕微轉變。對于化療藥物,有效的治療一致地將Tex-LAG3推向Tfh-DUSP4方向。
Ti分析一致顯示,在聯合治療后,Tfh增加,而Tex和增殖亞群減少,而對化療藥物有應答的患者表現出Tfh-DUSP4和Tem-GZMK的增加(圖4C)。這些結果表明,化療藥物減少了Tex,同時維持Tfh/Tex譜系處于中間狀態。然而,當與ATZ聯合使用時,特別是Nab-PTX+ATZ,能推動細胞狀態向Tfh方向發展,表明其對CD4+ T細胞亞群有顯著影響。
在接受Nab-PTX+ATZ有效治療后,觀察到從Treg到Tn-IL7R和Tfh-CXCR5的顯著樞紐轉移,而非應答者則表現出Tex和Treg的樞紐性增加(圖4I)。對于化療藥物,接受Nab-PTX治療的應答者表現出Tex的樞紐性降低,但Tfh-DUSP4、Treg、Tact、Tstr和Teff的樞紐性增加。相比之下,接受PTX治療的應答者表現出Treg和Tfh-DUSP4的樞紐性降低,同時Tn-CCR7和Teff的樞紐性增加(圖4I)。這些結果進一步證實了增強Tfh和Tn-IL7R,同時減少Treg和Tstr對于更好的治療反應的重要性。
7 肥大細胞對Nab-PTX相關治療的響應性擴增
肥大細胞在多種生理和病理過程中發揮復雜的作用,包括在腫瘤中,其傳統上被認為與免疫調節和促腫瘤效應有關。在TNBC中,肥大細胞是TME的關鍵介質,影響免疫反應和腫瘤生長。值得注意的是,作者在接受Nab-PTX治療的應答者中觀察到肥大細胞浸潤呈增加趨勢(圖5A、5B),但p值不顯著。
作者隨后利用小鼠4T1乳腺腫瘤模型來驗證Nab-PTX和抗PD-L1治療的效果。通過RNA-seq和scRNA-seq聯合分析,發現盡管這些治療之間的腫瘤大小沒有顯著差異,Nab-PTX治療后肥大細胞浸潤仍呈增加趨勢(圖5C)。Nab-PTX提高了Tn、Tcm、Tem和Treg的水平,同時Tex和Tfh呈上升趨勢,而抗PD-L1治療似乎提高了Tsem(圖5D)。這說明肥大細胞可能與T細胞的招募有關,特別是增強了Tn,隨后Tn轉變為Tem和功能失調的表型,而抗PD-L1治療則保留了Tsem并防止了T細胞功能障礙。
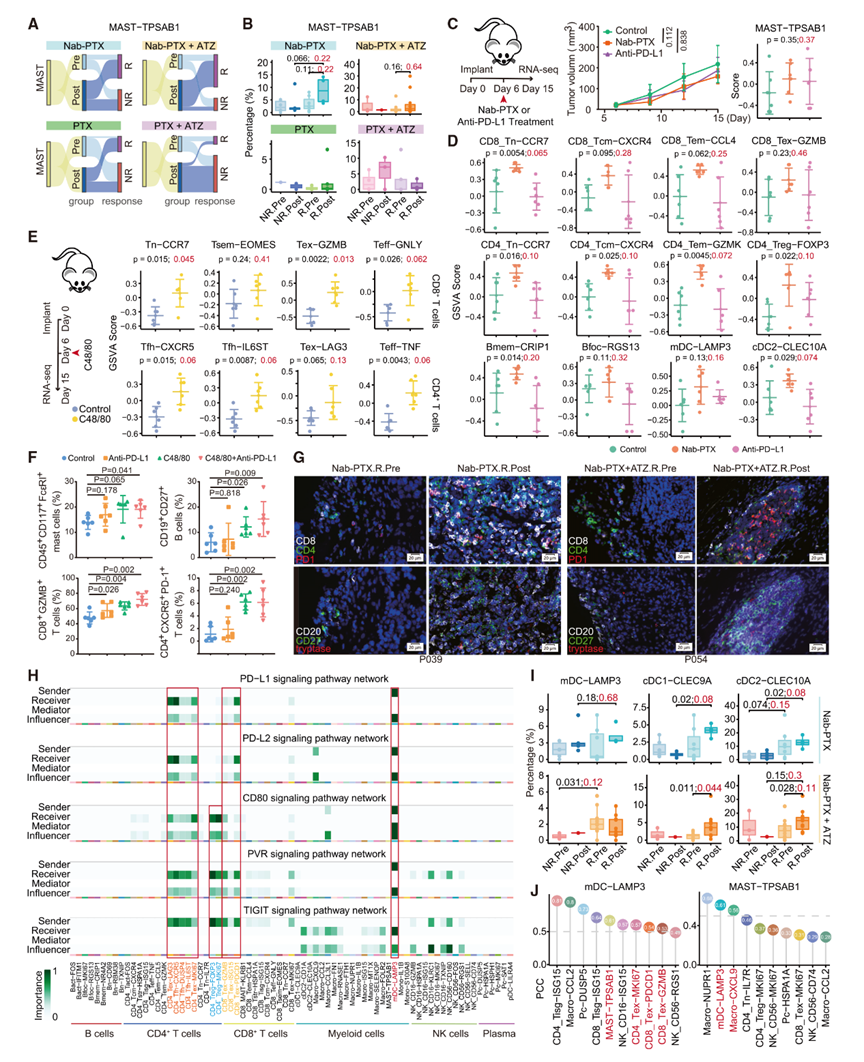
圖5:肥大細胞及其相關免疫細胞的動態變化
8 肥大細胞激活與T細胞反應及其關鍵調節因子的聯系
為了進一步揭示肥大細胞對TNBC腫瘤微環境的調節作用,作者用促進肥大細胞脫顆粒的陽離子激動劑48/80三鹽酸鹽(C48/80)處理同種異體小鼠腫瘤模型。在C48/80給藥對腫瘤生長影響有限的情況下,但作者仍觀察到肥大細胞水平升高,同時幼稚T細胞(Tn)、效應T細胞(Teff)、濾泡輔助T細胞(Tfh)和耗竭T細胞(Tex)也有所增加(圖5E),這進一步表明肥大細胞激活與TNBC腫瘤微環境中的T細胞反應密切相關。Tex的高比例可能解釋了對腫瘤生長影響有限的原因。為了在體內驗證肥大細胞與T細胞反應之間的聯系,作者進一步用抗PD-L1抗體、C48/80及其聯合治療小鼠。流式細胞分選(FACS)分析顯示,C48/80治療顯著增加了肥大細胞、CD8+ GZMB+ T細胞和CD4+ CXCR5+ PD-1+ T細胞(圖5F),從而鞏固了作者的結果。
CD27+ B細胞持續增加(圖5F)。作者還在對Nab-PTX和Nab-PTX+ ATZ有反應的臨床樣本上進行了多色免疫組化(IHC)染色,觀察到治療后肥大細胞和活化的T細胞及B細胞增加(圖5G)。值得注意的是,聯合治療還在TNBC中擴大了Bfoc(圖1G),突出了它們在Bfoc誘導中的作用。這些發現進一步強調了肥大細胞激活在塑造TNBC腫瘤微環境中免疫反應的作用。作者進一步分析了mDC與其他免疫細胞之間的配體-受體相互作用,揭示了其與Tex、Tfh和Treg通過CD274-PDCD1、CD80-CTLA4、NECTIN2-TIGIT和PVR-TIGIT等配對相互作用(圖5H)。這些發現突出了mDC在TNBC免疫景觀中的復雜作用。
9 肥大細胞在優化Nab-PTX聯合正反應治療中的重要性
為了進一步確認肥大細胞在促進對Nab-PTX+ATZ有效反應中的關鍵作用,作者用Nab-PTX聯合抗PD-L1抗體、肥大細胞脫顆粒穩定劑色甘酸鈉二鈉鹽(DSCG)以及Nab-PTX聯合抗PD-L1抗體和DSCG的組合治療小鼠4T1乳腺腫瘤模型(圖6E)。Nab-PTX聯合抗PD-L1治療顯著抑制了腫瘤生長。然而,當加入DSCG時,對腫瘤的療效變差,這進一步強調了肥大細胞在增強這種聯合治療有效性中的關鍵作用。
作者進一步進行了RNA-seq,以研究小鼠腫瘤微環境(TME)的動態變化,發現與DSCG聯合的治療增加了調節性或抑制性樹突狀細胞亞群,特別是成熟的樹突狀細胞(mDC)和表達CD1A的樹突狀細胞(cDC2-CD1A)(圖6F)。這些結果表明肥大細胞在調節抑制性樹突狀細胞亞群中具有雙重作用。此外,肥大細胞的抑制降低了Tn、中央記憶T細胞(Tcm)、干細胞樣效應記憶T細胞(Tsem)、濾泡輔助T細胞(Tfh)、B細胞前體(Bn)和漿細胞(Pc),同時增加了干擾素應答T細胞(Tisg)(圖6F)。總體而言,這些發現進一步強化了肥大細胞在調節對有效Nab-PTX和抗PD-L1治療至關重要的免疫群體中的關鍵作用。
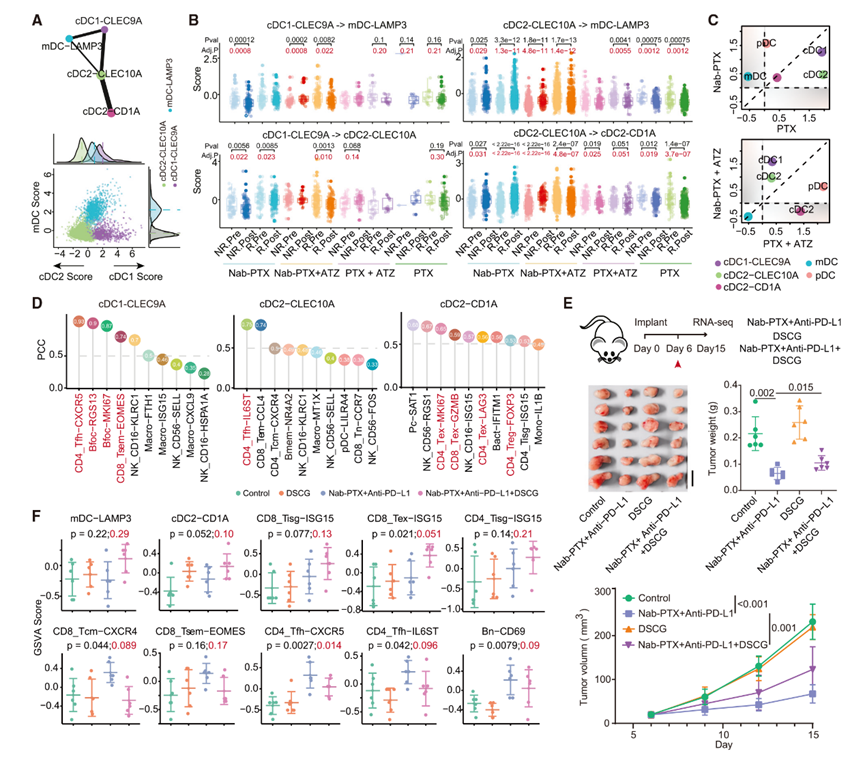
圖6:樹突狀細胞亞群的譜系聯系及動態變化
10 繪制TNBC中單核細胞/巨噬細胞的特征圖譜
SPP1是一種標記血管生成性巨噬細胞的標志物,由多個亞群表達,包括macro-CCL2、macro-MT1X、macro-RNASE1、macro-FN1和macro-ISG15。這些亞群通過分泌各種分子發揮調節功能,并參與SPP1、FN1和MIF等通路。具體來說,macro-CCL2表達SPP1和IL1RN,連接單核細胞和巨噬細胞,而macro-FN1和macro-MT1X在轉錄組上與macro-CCL2相似。Macro-MT1X和macro-RNASE1傾向于M2特征,而macro-CCL2和macro-ISG15表現出M1和M2的雙重特征(圖7A)。
基于細胞組成,作者構建了相關性網絡,并揭示了對Nab-PTX+ATZ有反應的腫瘤中共調控的模塊(圖7B)。作者根據特征亞群對這些模塊進行了分類,并在基線時識別出六個模塊,包括與Tex相關的模塊、與Tfh/Bfoc相關的模塊、干細胞樣相關的模塊、與Tn/Bn相關的模塊、增殖相關的模塊和應激相關的模塊。Macro-CXCL9位于與Tfh/Bfoc相關的模塊中,該模塊包含Tfh和Bfoc。Macro-CCL3L1在轉錄組上與macro-CXCL9相似,并與Tn-IL7R、Tfh和Tsem一起位于干細胞樣相關的模塊中(圖7B)。位于與Tex相關的模塊中的Macro-CCL2與Tex、Tisg和mDC一起,表現出具有促炎和抗炎雙重功能的特性。Macro-FOLR2、macro-NUPR1和macro-ISG15位于與Tn/Bn相關的模塊中,而macro-RNASE1與Treg和cDC2-CD1A相關。Macro-FN1和mono-S100A8位于包含增殖性Treg和Tex的增殖相關模塊中。這些相關性進一步突出了macro-CXCL9的促炎作用以及macro-RNASE1、macro-FN1和mono-S100A8的免疫抑制功能。
治療后,作者觀察到相關性景觀的顯著變化,樹突狀細胞在支持T細胞和B細胞反應方面的作用得到增強(圖7B)。作者識別出一個干細胞樣和與Tfh/Bfoc相關的模塊,包括Tfh、Tn-IL7R、Tsem、Bfoc、Bmem、cDC1、macro-FOLR2和macro-FTH1,以及一個包含Tfh-IL6ST、Bn和cDC2-CLEC10A的與Tfh/Bn相關的模塊。Macro-MT1X、macro-ISG15、mono-IL1B和cDC2-CD1A與Tex和Treg聚集在一起,而macro-FN1和mono-S100A8是應激相關模塊的一部分,突出了它們的免疫抑制作用。Macro-CCL2位于由IFN應答相關亞群組成的IFN相關模塊中,而macro-CCL3L1被發現在與Tn/Teff相關的模塊中,進一步強化了其促炎功能。
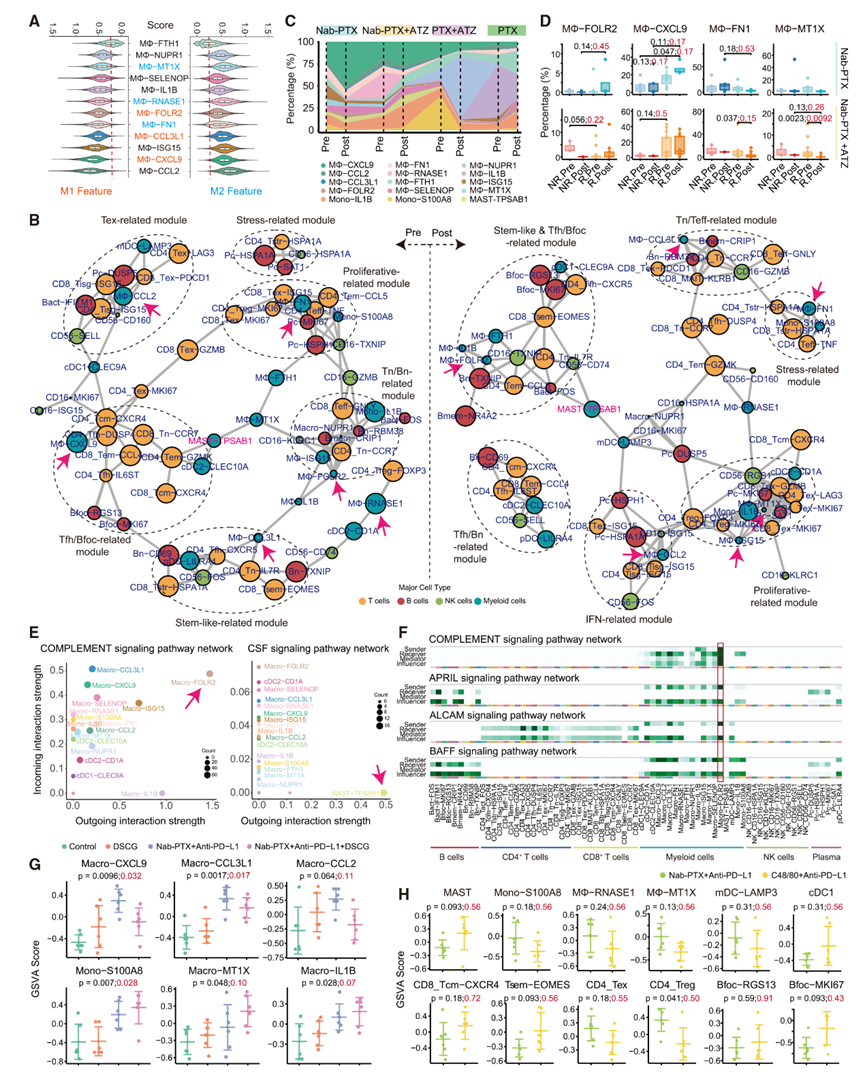
圖7:單核細胞/巨噬細胞的特征及其與肥大細胞的聯系
11 單核細胞/巨噬細胞對不同治療的動態反應
在對Nab-PTX+ATZ有反應的腫瘤中,作者觀察到免疫抑制性巨噬細胞水平下降,例如macro-FN1、macro-MT1X和macro-RNASE1,同時促炎性亞群如macro-CXCL9、macro-FOLR2和mono-IL1B水平上升(圖7C和圖7D)。Macro-FOLR2與人類乳腺癌中CD8+ T細胞浸潤相關的FOLR2+組織駐留巨噬細胞相似,與治療前和治療后的應答性腫瘤中的Tn和Bn聚集在一起(圖7B)。此外,macro-FOLR2可能通過補體系統促進其他巨噬細胞,特別是macro-CXCL9和macro-CCL3L1(圖7E和圖7F)。這些巨噬細胞共同影響T細胞和B細胞的招募和激活,可能通過CXC、主要組織相容性復合體II類(MHC-II)、增殖誘導配體(APRIL)、B細胞激活因子(BAFF)和活化白細胞細胞黏附分子(ALCAM)信號通路。
在應答者中,作者觀察到macro-FOLR2和macro-CXCL9水平上升,而mono-IL1B和免疫抑制性巨噬細胞如macro-FN1、macro-MT1X和macro-ISG15在Nab-PTX治療后下降(圖7C和圖7D),盡管p值未達到顯著性。類似地,PTX也提高了促炎性亞群如macro-FOLR2和macro-CCL3L1的水平,同時減少了包括macro-FN1、macro-MT1X、macro-ISG15和macro-RNASE1在內的免疫抑制性亞群(圖7C)。相比之下,PTX+ATZ傾向于減少macro-CXCL9和mono-S100A8,同時增加macro-NUPR1。這些發現表明,化療和Nab-PTX+ATZ均促進了促炎性巨噬細胞,同時減少了免疫抑制性亞群,營造了有利的免疫環境。
12 肥大細胞通過髓系細胞塑造TNBC的免疫景觀
肥大細胞在Nab-PTX+ATZ治療前后均與Tfh/Bfoc相關模塊表現出接近性(圖7B)。作者進一步分析了細胞間通信網絡,發現肥大細胞對髓系細胞產生了廣泛的影響(圖7E)。具體而言,肥大細胞主要向巨噬細胞和單核細胞發出信號,可能通過集落刺激因子(CSF)信號通路,以macro-FOLR2為主要受體。肥大細胞還與macro-CXCL9表現出共動態,并與macro-NUPR1和mDC呈正相關,但與macro-RNASE1、macro-MT1X和mono-IL1B呈負相關(圖5J),這表明它們在免疫調節中具有多面性作用,尤其是在協調巨噬細胞功能方面。
作者進一步分析了來自小鼠4T1乳腺腫瘤模型的RNA-seq數據,發現與單獨使用Nab-PTX和抗PD-L1治療相比,用DSCG抑制肥大細胞會減少促炎性巨噬細胞,如macro-CXCL9、macro-CCL3L1和macro-CCL2,同時增加免疫抑制性巨噬細胞,如macro-MT1X、macro-IL1B和mono-S100A8(圖7G)。這些發現表明肥大細胞參與免疫調節,可能通過增強促炎性巨噬細胞來發揮作用。
13 肥大細胞作為增強免疫檢查點阻斷(ICB)反應的新興治療靶點
基于這些發現,作者進一步探討了肥大細胞作為一種協同伙伴的潛力,旨在確定其激活是否能夠增強免疫檢查點阻斷(ICB)療法,特別是PD-L1阻斷的療效。鑒于Nab-PTX聯合抗PD-L1抗體的療效(圖6E),作者比較了C48/80或Nab-PTX與抗PD-L1抗體聯合在小鼠4T1乳腺腫瘤模型中的效果,發現兩種治療均顯著減少了腫瘤體積,其中C48/80聯合抗PD-L1抗體治療的腫瘤體積比Nab-PTX聯合抗PD-L1抗體治療更小,這表明通過激活肥大細胞增強抗PD-L1療法是一種有前景的治療策略。
此外,RNA-seq分析顯示,在C48/80聯合抗PD-L1治療后,包括Tsem、Tn-IL7R、Tcm、Bfoc和cDC1在內的幾種關鍵免疫細胞亞群水平增加(圖7H)。這些有益免疫細胞群體的增加伴隨著免疫抑制亞群的減少,如Tex、Treg、mDC、macro-MT1X和mono-S100A8。此外,FACS分析顯示,與單獨使用C48/80相比,C48/80聯合抗PD-L1治療后CD8+ GZMB+ T細胞和CD19+ CD27+ B細胞水平升高(圖5F)。總體而言,這些發現表明,肥大細胞的激活不僅增強了主要抗腫瘤免疫細胞,還重塑了腫瘤微環境,為有效的抗腫瘤治療創打下基礎。
結論:
綜上所述,作者揭示了人類TNBC和小鼠模型中肥大細胞通過促進T細胞和B細胞的招募和激活實現的在協調抗腫瘤免疫反應中的關鍵作用,發現與PD-L1阻斷聯合激活肥大細胞可減輕TNBC的進展。作者的研究結果提示肥大細胞是增強免疫檢查點阻斷(ICB)療法療效的有前景的輔助手段,這將為未來聯合療法的研究提供新的治療策略。
實驗方法:
小鼠腫瘤模型,scRNA-seq,TCR-seq,細胞培養,WB,免疫熒光,IHC
參考文獻:
Zhang Y, Chen H, Mo H, Zhao N, Sun X, Liu B, Gao R, Xu B, Zhang Z, Liu Z, Ma F. Distinct cellular mechanisms underlie chemotherapies and PD-L1 blockade combinations in triple-negative breast cancer. Cancer Cell. 2025 Jan 30:S1535-6108(25)00025-X. doi: 10.1016/j.ccell.2025.01.007. Epub ahead of print. PMID: 39919737.