腫瘤源性外泌體LINC01812誘導M2巨噬細胞極化促進膽管癌的神經周圍浸潤
M2型巨噬細胞在侵襲性實體瘤的腫瘤微環境中發揮著關鍵作用。它們與神經周圍浸潤(PNI)密切相關,且常與不良預后相關聯。在此背景下,腫瘤源性外泌體是細胞間通訊的重要介質。然而,腫瘤細胞誘導的M2型巨噬細胞與膽管癌中的PNI之間的關系尚未得到探究。在本研究中,我們運用多重免疫熒光和轉錄組測序技術,證明了LINC01812在膽管癌組織中表達上調,且其與M2型巨噬細胞浸潤呈正相關。外泌體lncRNA測序、外泌體攝取實驗、RNA下拉實驗以及質譜分析表明,巨噬細胞能夠攝取含有LINC01812的外泌體,并促進膽管癌細胞向M2型表型轉化。此外,腫瘤微環境可通過M2型巨噬細胞顯著增強膽管癌細胞的神經浸潤能力。本研究結果表明,源自膽管癌的含LINC01812的外泌體可誘導M2型巨噬細胞極化,并促進神經浸潤,從而為治療膽管癌中的PNI提供了新的潛在治療靶點。本文于2025年3月發表于“Cancer Letters”(IF=9.1)上。
技術路線:

結果:
1)CCA不同浸潤階段M1/M2巨噬細胞密度
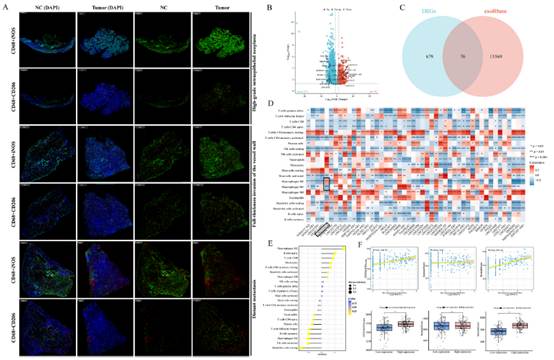
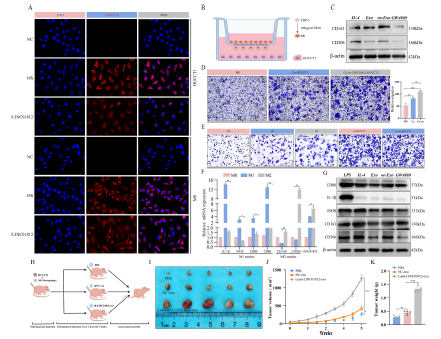
我們采用多重熒光染色技術,檢測了CD68、iNOS和CD206之間的關系。結果顯示,M1型巨噬細胞呈廣泛陽性信號,且在腺體組織中顯著聚集。相比之下,M2型巨噬細胞在腫瘤侵襲前沿的微環境中分布更為彌散。為驗證免疫熒光染色結果,我們對iNOS和CD206的熒光強度與細胞密度進行了定量分析。結果表明,與鄰近正常組織相比,腫瘤組織中iNOS的熒光強度和M1型巨噬細胞的密度均顯著降低,而CD206的熒光強度和M2型巨噬細胞的密度則顯著升高(圖1A)。隨后,我們對12例膽管癌(CCA)患者的樣本進行了全轉錄組測序。我們與exoRbase數據庫進行了聯合分析,并鑒定出76個差異上調的差異表達基因(DEGs)(圖1B和C)。其中,LINC01812尤為引人關注,因為它在膽管癌組織中的表達顯著升高,且在膽管癌患者來源的外泌體中富集,提示其在腫瘤-免疫細胞通訊中可能發揮作用。我們觀察到LINC01812的表達與M2型巨噬細胞浸潤呈正相關,與M1型巨噬細胞水平呈負相關,這支持了其可能參與免疫細胞分化和功能調節(圖1D)。此外,我們利用公共數據庫驗證了LINC01812與M2型巨噬細胞之間的正相關性(圖1E)。此外,我們證實了LINC01812高表達患者的基質評分和ESTIMATE評分顯著高于LINC01812低表達患者(圖1F)。基于這些結果,我們選擇LINC01812進行進一步研究,以闡明其在膽管癌中的功能作用和分子機制。
2)THP-1細胞外泌體的分離、表征和攝取
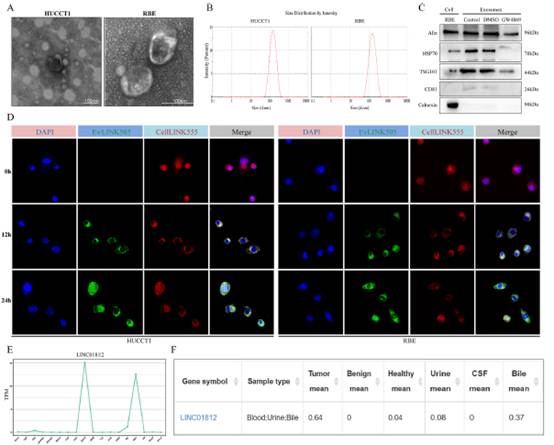
TEM圖像顯示,外泌體呈現出典型的杯狀形態(圖2A)。NTA顯示,分離得到的外泌體的平均直徑約為110 nm,與典型外泌體的特征一致(圖2B)。Western blot實驗證實了外泌體標志物(包括Alix、HSP70、TSG101、CD81)以及陰性標志物calnexin的表達(圖2C)。共聚焦顯微鏡顯示,隨時間推移,積累在THP-1細胞周圍的外泌體數量顯著增加(圖2D)。用于分析外泌體中LINC01812表達的exoRbase數據庫顯示,其在膽汁、食管鱗狀細胞癌和黑色素瘤中的表達水平升高(圖2E)。此外,腫瘤患者血液、尿液和膽汁樣本中的LINC01812表達顯著高于健康對照組(圖2F)。
3)LINC01812促進CCA細胞的增殖、遷移和侵襲
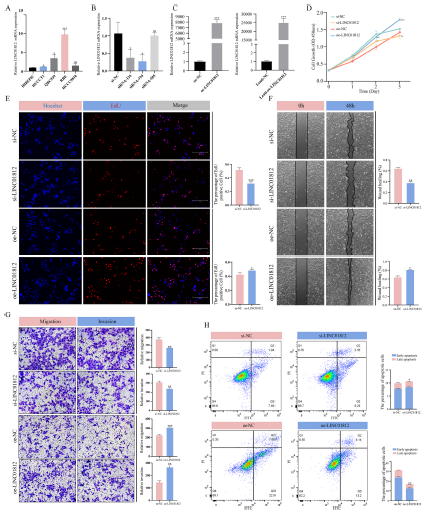
為探究LINC01812在CCA中的功能作用,我們首先評估了其在HIBEPIC、HUCCT1、QBC939、RBE和HCCC9810細胞中的表達水平(圖3A)。根據qPCR分析結果,選擇RBE細胞系進行LINC01812敲低實驗,并利用慢病毒載體在HUCCT1細胞中建立了LINC01812的穩定過表達細胞系(圖3B和C)。CCK-8和EdU實驗結果顯示,LINC01812敲低顯著抑制了RBE細胞的增殖(圖3D和E)。劃痕愈合實驗和Transwell實驗進一步表明,LINC01812敲低顯著降低了CCA細胞的遷移和侵襲能力(圖3F和G)。流式細胞術結果顯示,LINC01812敲低后細胞凋亡顯著增加。相反,在HUCCT1細胞中過表達LINC01812則產生了與敲低相反的效果;LINC01812過表達顯著促進了細胞增殖(圖3D)、遷移和侵襲(圖3F和G);此外,還降低了細胞凋亡率。
4)CCA細胞外泌體衍生的LINC01812誘導M2巨噬細胞極化,促進腫瘤進展
通過FISH技術檢測了LINC01812在CCA細胞和巨噬細胞中的亞細胞定位。結果顯示,LINC01812主要定位于細胞質中(圖4A)。采用Transwell共培養模型將HUCCT1細胞與M0型巨噬細胞共培養(圖4B和D)。與LINC01812過表達的HUCCT1細胞共培養后,M0型巨噬細胞的遷移能力顯著增強。Western blot分析證實,在此共培養條件下,M0型巨噬細胞發生了M2型極化(圖4C)。僅與外泌體共培養的結果顯示,Lenti-oe-LINC01812-exo顯著誘導M0型巨噬細胞分化為M2型而非M1型巨噬細胞(圖4E和G)。此外,添加外泌體抑制劑GW4869顯著抑制了CCA細胞來源的外泌體誘導的M0型巨噬細胞極化。qPCR證實,M2型巨噬細胞中LINC01812的表達顯著上調(圖4F)。在裸鼠皮下成瘤實驗中,研究了外泌體來源的LINC01812在CCA體內的作用(圖4H)。結果顯示,與NC-exo組相比,Lenti-oe-LINC01812-exo組的腫瘤體積和重量顯著增加;而NC-exo組的腫瘤大小和重量相對于PBS組也顯著增加(圖4I、J、4K)。
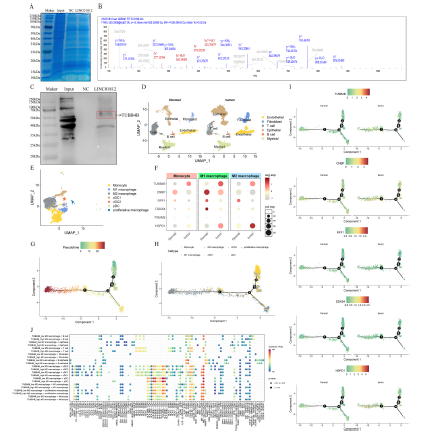
5)外泌體LINC01812通過與TUBB4B相互作用促進M2巨噬細胞極化
我們使用生物素標記的LINC01812探針或陰性對照(NC)探針與來自THP-1 M0型巨噬細胞的總蛋白提取物進行孵育,以探究LINC01812的作用機制。利用鏈霉親和素磁珠進行下拉分析后,通過SDS-PAGE分離蛋白產物(圖5A)。采用質譜(MS)技術鑒定LINC01812結合蛋白,并選取至少兩條獨特鑒定的肽段進行進一步分析。候選蛋白包括TUBB4B、CNBP、RPF1、DDX54、PGAM2和HSPD1。利用基因表達綜合數據庫的單細胞數據對腫瘤微環境(TME)中的巨噬細胞浸潤情況進行表征。首先,將所有細胞聚類為六個亞群(圖5D),并將髓系亞群進一步重新聚類為單核細胞、M1型巨噬細胞和M2型巨噬細胞(圖5E)。隨后,我們分析了重新聚類的巨噬細胞亞群中TUBB4B、CNBP、RPF1、DDX54、PGAM2和HSPD1的表達水平。結果顯示,與鄰近組織相比,TUBB4B和HSPD1在癌組織中顯著高表達,而PGAM2的表達無顯著差異。因此,我們對剩余五個基因進行了擬時序分析。擬時序分析用于模擬CCA中髓系細胞的分化過程(圖5G和H),結果顯示單核細胞處于分化的早期階段;經過分支點4后,它們逐漸分化為M1型和M2型巨噬細胞。隨后,我們分析了這些結合蛋白在M2型巨噬細胞分化擬時序軌跡上的表達趨勢(圖5I)。結果表明,TUBB4B是LINC01812調控M2型巨噬細胞分化過程中的關鍵基因。分析了TUBB4B高表達組和低表達組之間的配體-受體介導的細胞相互作用(圖5J)。Western blot分析驗證了TUBB4B與LINC01812之間的相互作用(圖5C),二級質譜圖如圖5B所示。
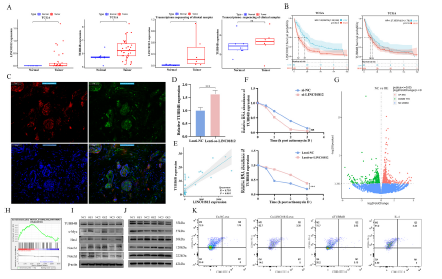
6)外泌體LINC01812通過結合TUBB4B調控Notch通路
與鄰近的非癌組織相比,在12例CCA樣本和TCGA數據庫的腫瘤組織中,LINC01812和TUBB4B均顯著上調(圖6A)。在TCGA-CHOL隊列中,LINC01812的高表達與較差的總生存率相關;然而,TUBB4B的表達并未顯示出顯著的預后差異(圖6B)。隨后,我們進行了原位雜交和雙重免疫熒光染色,以確定LINC01812和TUBB4B在CCA組織中的共定位情況。我們還使用免疫熒光技術分析了TUBB4B和M2型巨噬細胞極化標志物CD206的定位情況。結果顯示,LINC01812和TUBB4B在腫瘤組織中共定位(圖6C)。然而,由于CD206在腫瘤組織中廣泛分布,TUBB4B與CD206的共定位并不顯著。這些發現表明LINC01812和TUBB4B的表達水平之間可能存在相關性。對來自患者的40例CCA組織樣本進行的qPCR驗證了這些結果(圖6E)。在THP-1 M0型巨噬細胞中過表達LINC01812可增加TUBB4B的表達(圖6D)。我們用放線菌素D處理了LINC01812過表達和敲低的M0型巨噬細胞,以探究LINC01812在調控TUBB4B中的作用。如圖6F所示,在放線菌素D處理下,LINC01812過表達顯著增加了TUBB4B的mRNA表達。相反,在相同實驗條件下,LINC01812的敲低導致TUBB4B表達顯著降低(圖6F)。利用siRNA轉染THP-1來源的M0型巨噬細胞,以敲低TUBB4B。轉染48小時后,進行RNA測序分析,鑒定出1626個差異表達基因(DEGs)(圖6G)。GSEA顯示,在TUBB4B過表達組中,Notch通路基因集的表達水平較高(圖6H)。Western blot分析顯示,與NC組相比,在Lenti-oe-LINC01812過表達組中,TUBB4B和Notch通路成分(包括c-Myc、Hes1、Notch1和Notch3)的表達顯著增加(圖6I)。LINC01812誘導的Notch通路激活依賴于TUBB4B的表達,且敲低TUBB4B可有效阻斷LINC01812誘導的Notch通路激活。這表明LINC01812與TUBB4B之間存在線性調控軸(圖6J)。最后,流式細胞術顯示,與NC組相比,用Lenti-oe-LINC01812-exo處理的M0型巨噬細胞顯著向M2表型分化;然而,在M0型巨噬細胞中敲低TUBB4B顯著抑制了Lenti-oe-LINC01812-exo的作用(圖6K)。
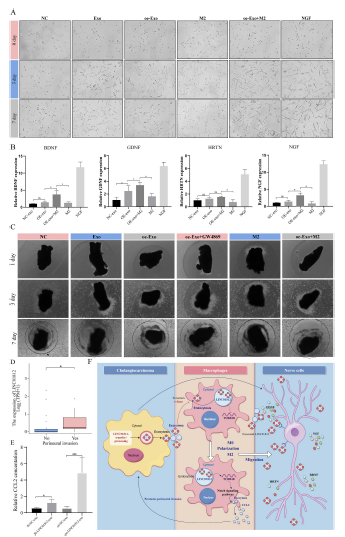
7)外泌體LINC01812通過誘導M2巨噬細胞極化促進PNI
外泌體可被神經元細胞攝取,并影響特定神經營養因子的分泌。因此,我們評估了在不同處理條件下PC12細胞的分化水平以及四種特定神經營養因子的分泌情況。外泌體可促進低分化PC12細胞的分化,而Lenti-oe-LINC01812-exo可進一步增強這種效果。與M2型巨噬細胞共培養可放大分化效應,使分化水平顯著升高(圖7A)。qPCR結果顯示,與NC-exo處理組相比,經Lenti-oe-LINC01812-exo處理的PC12細胞中神經營養因子的分泌水平略有增加,盡管差異無統計學意義;然而,當PC12細胞與M2型巨噬細胞共培養時,這種效應顯著增強(圖7B)。我們建立了體外CCA周圍神經浸潤(PNI)模型,通過觀察CCA細胞在基質膠中的遷移情況,進一步探索外泌體的作用。外泌體可促進CCA細胞向背根神經節(DRG)的侵襲。與M2型巨噬細胞共培養可顯著增強這種侵襲能力,而預先用GW4869處理CCA細胞則可有效抑制這一過程(圖7C)。這表明外泌體LINC01812和M2型巨噬細胞可以通過獨立和協同機制促進PNI。TCGA-CHOL數據顯示,PNI患者的LINC01812表達水平顯著升高(圖7D)。在確認巨噬細胞中的Notch通路可被外泌體LINC01812激活后,我們進行了ELISA以測量巨噬細胞上清液中CCL2的表達水平。經Lenti-oe-LINC01812-exo處理后,CCL2表達增加了約五倍。相比之下,經NC-exo處理的巨噬細胞中CCL2表達僅增加了1.6倍,這可能是由于其他補償機制對CCL2的調控所致(圖7E)。此外,本研究的作用機制示意圖如圖7F所示。
結論:
本研究證明,CCA細胞來源外泌體可通過LINC01812-Notch-CCL2軸介導M2型巨噬細胞極化并促進神經浸潤。這一過程形成了有利于腫瘤侵襲的免疫微環境,并突顯了LINC01812作為膽管癌神經浸潤預測生物標志物的潛力。
實驗方法:
qPCR,CCK8,傷口愈合試驗,Transwell,流式,FISH,Western blotting,RNA pull-down。
參考文獻:
Wang Q, Sun Z, Guo J, Li H, Zhang J, Zhang B, Zhou B, Feng Y. Tumor-derived exosomal LINC01812 induces M2 macrophage polarization to promote perineural invasion in cholangiocarcinoma. Cancer Lett. 2025 May 1;617:217596. doi: 10.1016/j.canlet.2025.217596.