糖尿病傷口愈合障礙新機制:中性粒細胞胞外誘捕網(NETs)通過內質網應激誘發成纖維細胞鐵死亡
糖尿病患者傷口延遲愈合顯著增加截肢和全身感染的風險。然而,其潛在的分子機制尚不清楚。成纖維細胞通過分泌膠原蛋白參與創面修復,其功能障礙會嚴重影響創面愈合和組織再生。越來越多的證據表明,中性粒細胞胞外誘捕網(NETs)的過度產生會加劇局部炎癥并誘導細胞死亡,從而延遲傷口愈合。盡管有這些發現,NETs導致傷口愈合障礙的確切機制仍不清楚。本研究利用體外和體內模型來研究NETs通過內質網應激促進成纖維細胞鐵死亡并促進受損糖尿病傷口愈合的分子機制。我們的研究結果表明,NETs誘導成纖維細胞的鐵死亡,從而損害其膠原分泌能力。我們進一步證明了IRE1α/XBP1,一個關鍵的內質網應激通路,參與了NETs誘導的成纖維細胞鐵死亡。此外,靶向該通路可顯著促進糖尿病創面愈合。這些發現為治療難治性糖尿病創面提供了新的分子靶點和潛在的治療策略。該研究于2025年5月發表在《Free Radical Biology and Medicine》,IF:8.2。
技術路線
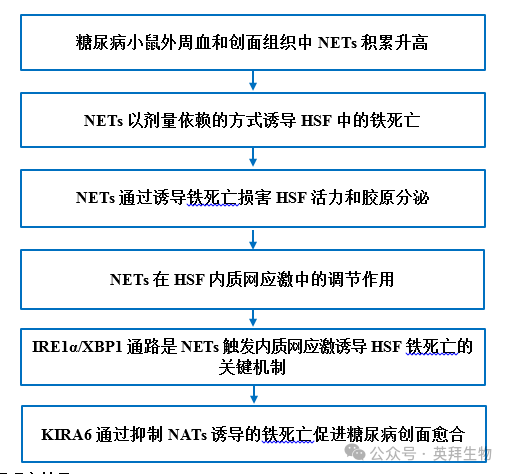
主要研究結果:
1.糖尿病小鼠外周血和創面組織中NETs積累升高
為研究NETs在糖尿病創面愈合中的作用,我們建立了糖尿病小鼠模型,并評估了NETs生物標志物CitH3和MPO在創面組織和外周血中的表達水平。代表性免疫熒光圖像顯示,與對照組小鼠相比,糖尿病小鼠創面皮膚中CitH3和MPO的浸潤顯著增加(圖1A)。對外周血中NETs水平的分析表明,糖尿病小鼠中的CitH3和MPO水平顯著高于健康對照小鼠(圖1B和C)。這些結果表明,在糖尿病條件下,外周血和創面組織中存在廣泛的NETs蓄積,表明NETs在糖尿病慢性創面的發病機制中是必不可少的。
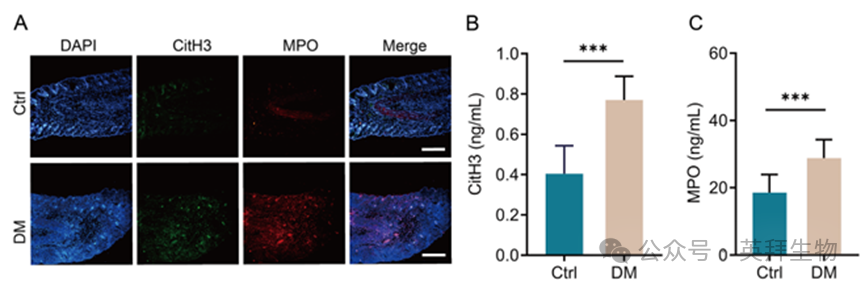
圖1.糖尿病小鼠傷口組織和外周血中NETs積累升高
2.NETs以劑量依賴的方式誘導人皮膚成纖維細胞(HSF)中的鐵死亡
在本文中,我們使用中性粒細胞分離試劑盒從健康志愿者的外周血中分離中性粒細胞,并將其與100 nM PMA孵育4 h以誘導NETs形成(圖2A)。隨后使用免疫熒光觀察NETs的形成(圖2B)。我們利用微陣列基因表達譜進行了轉錄組學分析,以檢測NETs對成纖維細胞功能的影響及其潛在的調控機制。火山圖顯示,與對照組相比,NETs處理組有657個上調和371個下調的DEGs(圖2C)。熱圖分析顯示,PTGS2是NETs處理后上調最顯著的基因之一,表明其在鐵死亡調節中的潛在作用(圖2D)。為驗證這些轉錄組學發現,我們評估了用逐漸增加濃度的NETs(0、25、50和100 μg/mL)處理24 h的HSF細胞中PTGS2和SLC7A11(鐵死亡的關鍵調節因子)的mRNA水平。此外,qPCR顯示PTGS2 mRNA水平呈劑量依賴性上調(圖2E),而SLC7A11 mRNA表達隨NETs濃度的增加而顯著下調(圖2F)。NETs處理以濃度依賴性方式顯著降低HSF活力(圖2G)。NETs暴露后LPO水平顯著升高(圖2H),而GSH水平以劑量依賴性方式降低(圖2I)。透射電鏡顯示經nets處理的HSF中存在嚴重的線粒體損傷,包括線粒體萎縮、嵴斷裂和膜完整性受損(圖2J)。WB分析證實,NETs處理后PTGS2表達顯著上調,而SLC7A11水平降低(圖2K-M)。此外,關鍵ECM蛋白,COL I和COL III,以劑量依賴性方式顯著下調(圖2N-P)。這些結果表明,NETs以劑量依賴性方式誘導HSF發生鐵死亡,損害其膠原分泌能力。
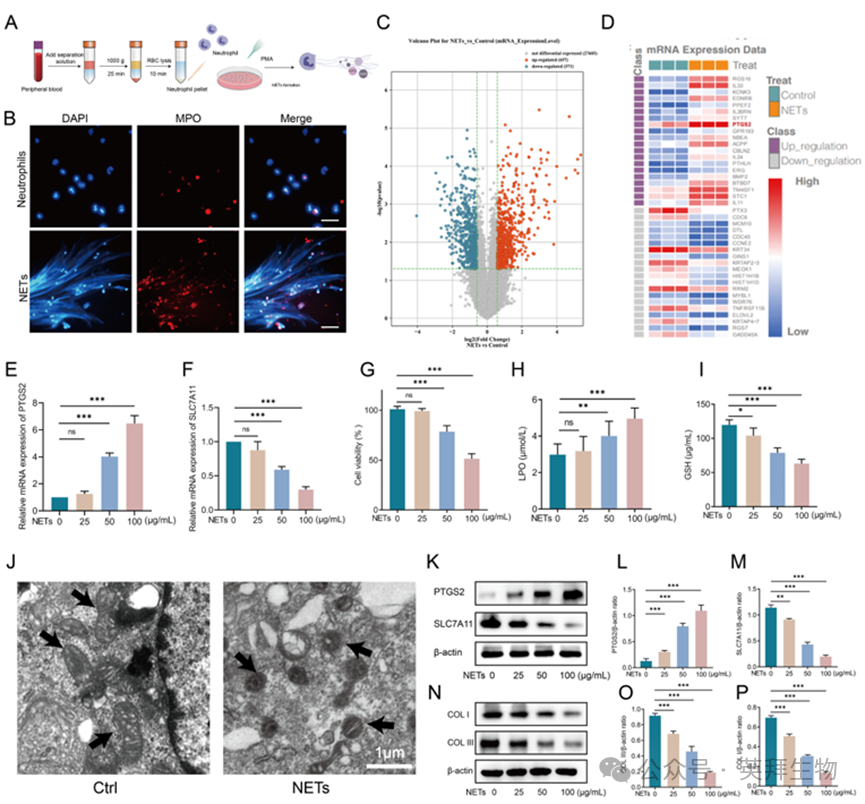
圖2.NETs可誘導HSF發生鐵死亡
3. NETs通過誘導鐵死亡損害HSF活力和膠原分泌
為探討鐵死亡在NETs誘導的細胞功能障礙中的作用,我們研究了鐵死亡抑制劑ferrostatin-1 (Fer-1)對NETs誘導的HSF細胞功能障礙的影響。我們發現,NETs顯著增加細胞內Fe2+水平,與鐵死亡誘導劑Erastin相當,而Fer-1預處理有效地緩解了這一效應(圖3A)。同樣,Fer-1預處理顯著減少了ROS的積累(圖3B)。NETs處理顯著增加了PTGS2和ACSL4的表達,同時降低了COL I、COL III、GPX4和SLC7A11(圖3C-I)。Fer-1有效地逆轉了這些作用。使用C11 LPO探針的流式細胞術(圖3J)以及LPO和谷胱甘肽GSH水平的測定(圖3K和L)進一步證實,NETs在HSF中誘導LPO。正如預期的那樣,Fer-1有效地減輕了NETs對HSF的影響。Fer-1預處理減輕了NETs誘導的細胞毒性,這可以通過提高細胞活力得到證明(圖3M)。這些結果表明,NETs通過增加LPO和降低抗氧化能力促進成纖維細胞鐵死亡,可能導致細胞死亡和功能障礙。
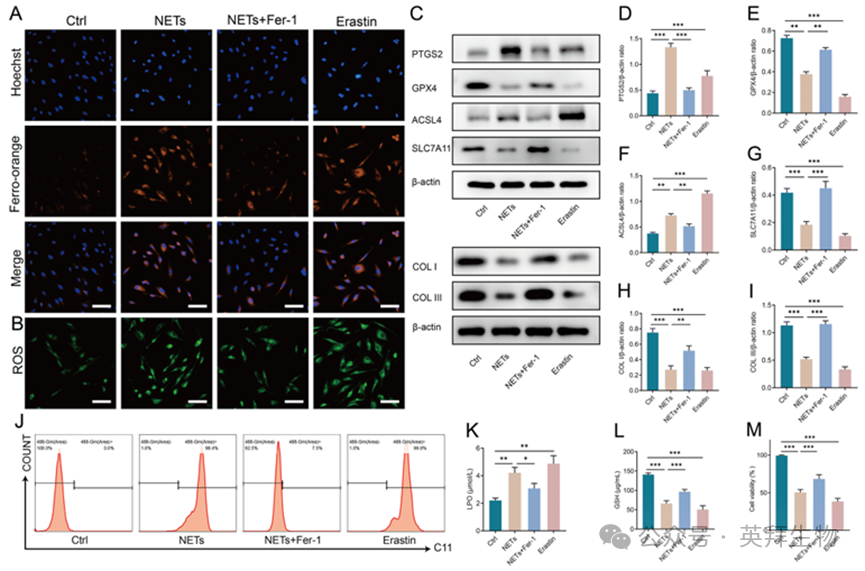
圖3.抑制鐵死亡可減輕NETs誘導的HSF功能障礙并恢復細胞活力
4. NETs在HSF內質網應激中的調節作用
內質網應激是細胞內ROS和LPO積累的重要調控途徑。因此,我們假設NETs通過激活內質網應激來調節HSF的鐵死亡。透射電鏡分析顯示,與對照組相比,NETs處理組線粒體出現鐵死亡(圖4A,黑色箭頭),同時粗面內質網顯著擴張(圖4A,白色箭頭),表明內質網應激的激活。我們進一步分析了三個主要的內質網應激感受器:ATF6, IRE1α和PERK的激活。WB分析顯示,與對照組相比,NETs處理顯著增加了IRE1α和PERK的磷酸化,而ATF6的表達沒有變化(圖4B-E)。這些發現表明,NETs主要通過IRE1α和PERK途徑而不是ATF6途徑誘導內質網應激。
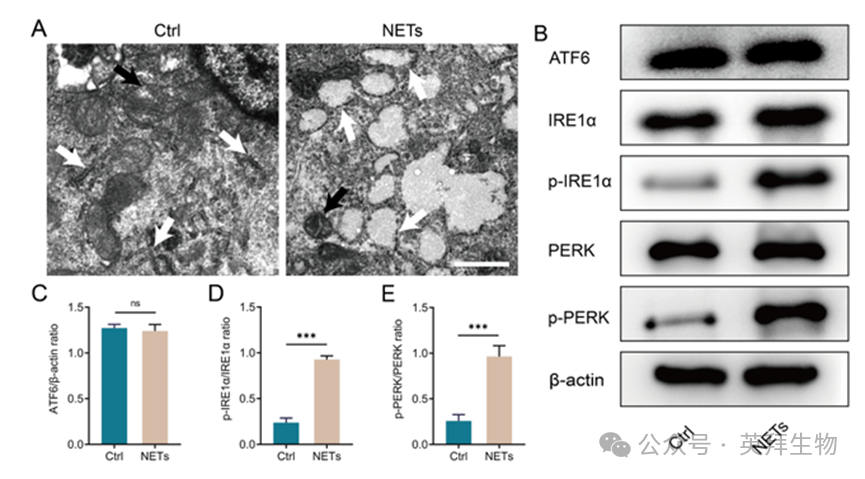
圖4.NETs在體外激活內質網應激
5.IRE1α/XBP1通路是NETs觸發內質網應激誘導HSF鐵死亡的關鍵機制
為進一步研究IRE1α和PERK通路在鐵死亡中的調控作用,我們用IRE1α抑制劑(KIRA6, 10 μM)、PERK抑制劑(GSK2606414, 2 μM)和鐵死亡抑制劑(Fer-1, 15 μM)預處理HSF,然后用NETs處理24 h。采用ER-Tracker評估內質網擴張情況。熒光圖像顯示,經NETs處理的HSF中,ER熒光強度明顯增強,而經KIRA6或GSK2606414預處理后,ER熒光強度減弱。相反,Fer-1預處理沒有顯著改變NETs處理的HSF中的ER熒光強度(圖5A)。NETs + KIRA6組ROS水平明顯降低,細胞存活率升高。GSK2606414對ROS積累的抑制作用不如KIRA6顯著(圖5B),對細胞活力的影響最小(圖5C)。這些結果表明,抑制鐵死亡不影響NETs誘導的內質網擴張。PERK通路對NETs誘導的脂質過氧化的調節作用很小。WB分析顯示,KIRA6預處理的HSF中,PTGS2表達降低;而SLC7A11表達增加。GSK2606414預處理的NETs組中PTGS2和SLC7A11的表達水平無明顯變化。Fer -1預處理的NETs組中IRE1α和PERK表達水平保持不變(圖5D-H)。這些結果表明,NETs主要通過IRE1α通路的激活來調節內質網應激,從而影響HSF的鐵死亡。雖然NETs激活了PERK通路,但它們對HSF的鐵死亡沒有顯著的調節作用。Fer-1對內質網擴張和內質網應激通路蛋白的表達無顯著影響,表明NETs誘導的HSF鐵死亡主要受IRE1α通路的調控。
為研究NETs是否通過激活IRE1α/XBP1通路促進HSF的鐵死亡,我們使用FerroOrang染色檢測細胞內Fe2+的積累。FerroOrange的熒光圖像顯示,KIRA6可以抑制HSF中NETs誘導的細胞內Fe2+的積累(圖5I)。WB分析顯示,NETs刺激顯著上調了HSF中XBP1和CHOP的表達,表明內質網應激的IRE1α/XBP1軸被激活。KIRA6預處理可抑制ACSL4的表達,同時恢復GPX4的表達(圖5J-N)。透射電鏡顯示NETs處理后細胞內質網和線粒體超微結構發生明顯改變。與NETs處理組相比,KIRA6預處理減輕了HSF的內質網擴張,并顯著恢復了線粒體形態和超微結構(圖5O)。流式細胞術分析顯示,KIRA6抑制了NETs誘導的HSF脂質過氧化(圖5P)。我們的研究結果表明,NETs通過激活IRE1α/XBP1通路觸發HSF中內質網應激介導的鐵死亡。
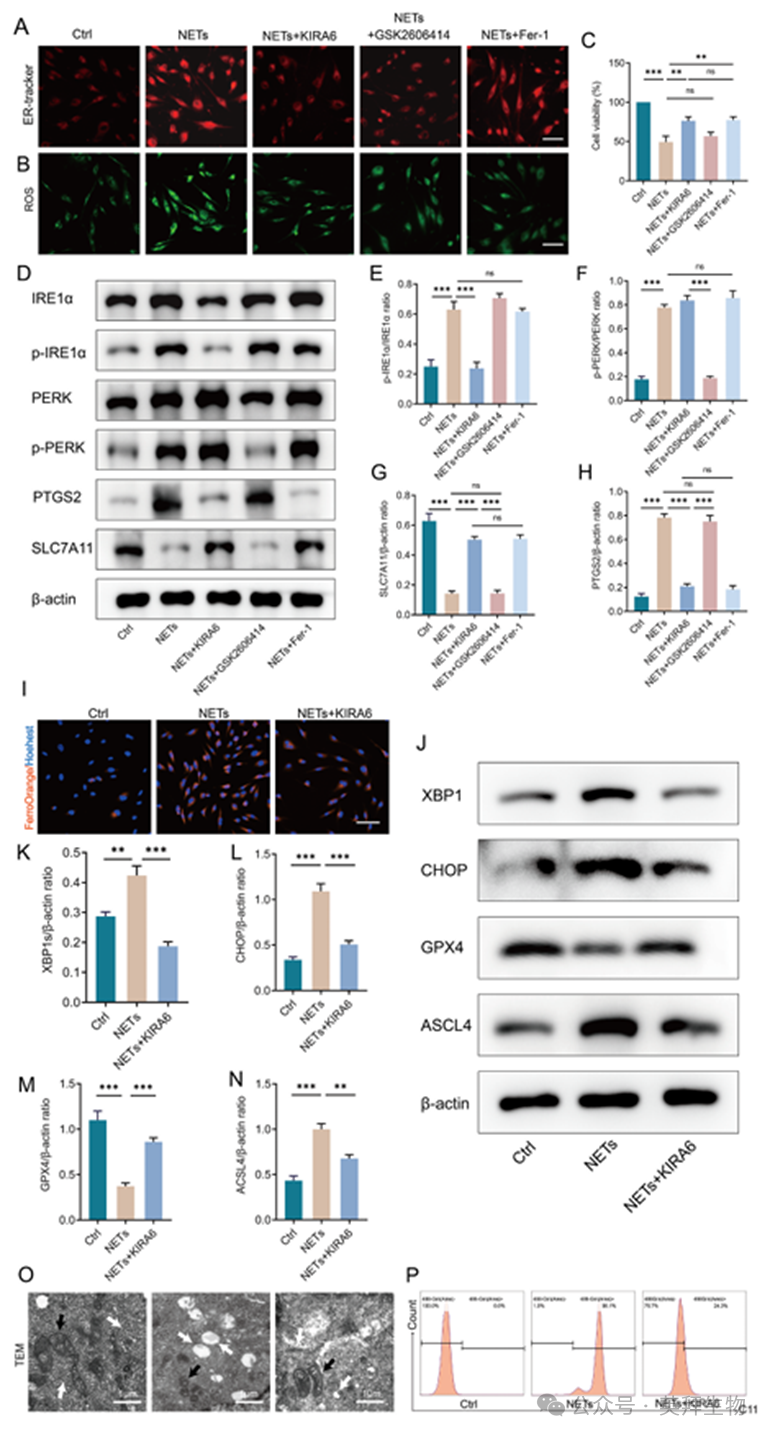
圖5.IRE1α/XBP1通路是NETs觸發內質網應激誘導HSF鐵死亡的關鍵介質
6.KIRA6通過抑制NETs誘導的鐵死亡促進糖尿病創面愈合
我們創建了糖尿病小鼠傷口愈合模型,并在14天內監測傷口愈合情況,以評估NETs誘導的鐵死亡對傷口愈合的影響(圖6A)。不同時間點(0、3、7和14天)的代表性傷口圖像表明,與未經治療的糖尿病小鼠相比,DM + KIRA6組小鼠的傷口閉合改善(圖6B和C)。此外,KIRA6處理顯著增強了皮膚創面ⅰ型膠原的表達,恢復了皮膚的膠原分泌能力。此外,內質網應激相關標志物(IRE1α, XBP1和CHOP)的表達下降,伴隨脂質過氧化相關蛋白PTGS2和ACSL4的下調和抗氧化蛋白GPX4的上調(圖6D)。這些結果表明,KIRA6通過抑制NETs誘導的鐵死亡來減輕糖尿病慢性創面。
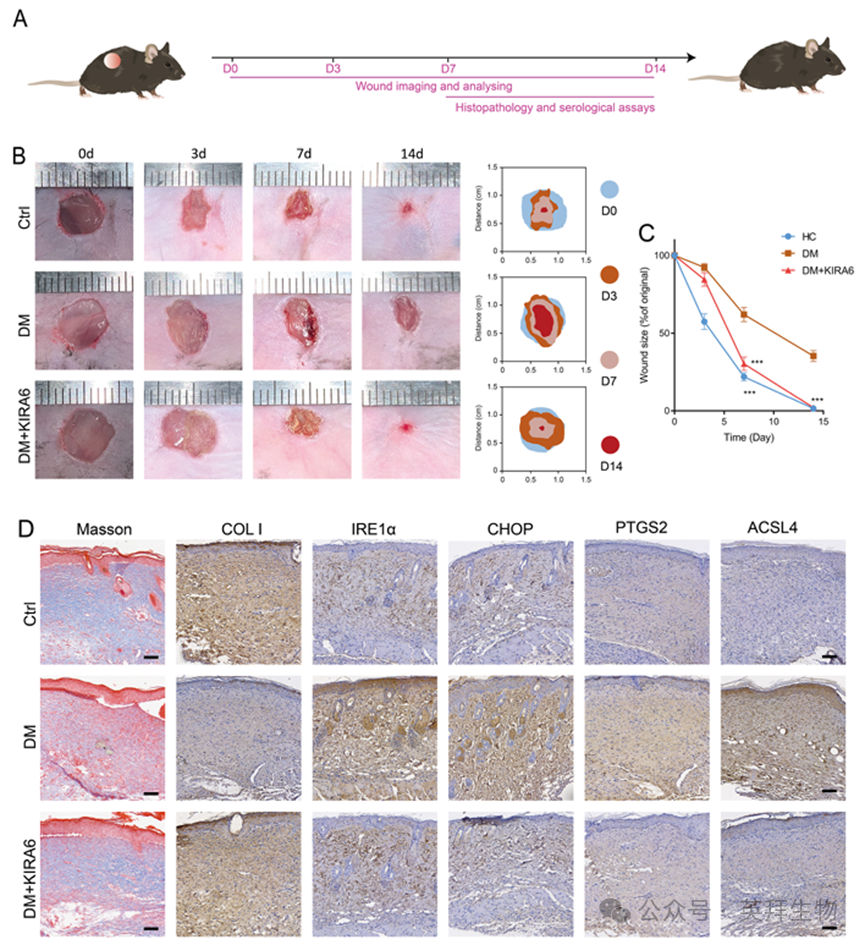
圖6.KIRA6通過抑制鐵死亡促進體內糖尿病創面愈合
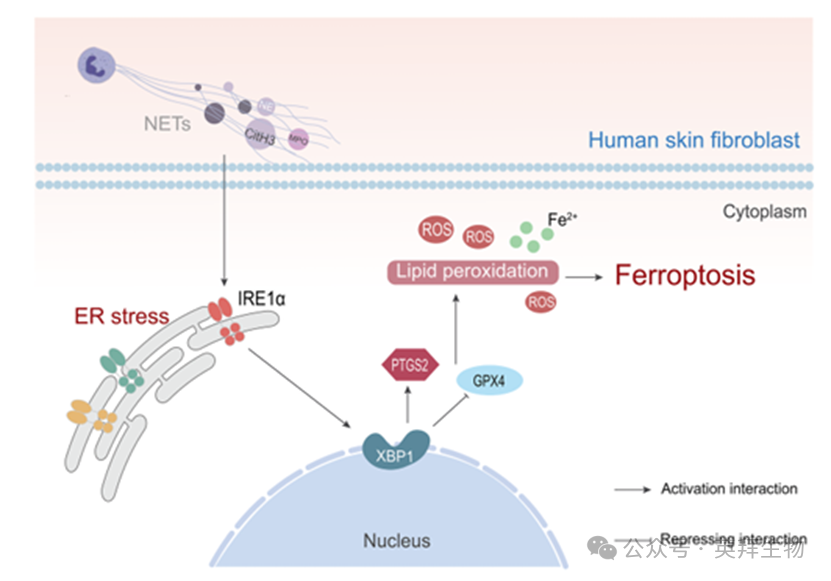
圖7.示意圖總結。NETs通過IRE1α/XBP1通路加劇脂質過氧化和ROS釋放,從而誘導HSF發生鐵死亡。
結論
綜上所述,我們通過體內和體外模型證明了NETs在糖尿病傷口延遲愈合中的作用。具體而言,NETs通過激活IRE1α/XBP1信號通路啟動內質網應激,導致HSF發生鐵死亡,損害成纖維細胞的修復功能(圖7)。此外,KIRA6治療有效地減輕了NETs誘導的細胞損傷,并顯著促進傷口愈合。調節NETs觸發內質網應激誘導細胞死亡的分子機制是緩解糖尿病傷口延遲愈合的一種有前景的治療策略。
參考文獻
Zhao H, Liu Y. Neutrophil extracellular traps induce fibroblast ferroptosis via IRE1α/XBP1-mediated ER stress to impair diabetic wound healing. Free Radic Biol Med. 2025 Aug 16;236:17-27. doi: 10.1016/j.freeradbiomed.2025.05.391. Epub 2025 May 14. PMID: 40379156.